|
|
|
MRGde
KONTRAST MADDELER
80li yılların ikinci yarısı MRGnin
radyolojide inceleme yöntemleri arasına girmesinin altın
yılları oldu; bunun en büyük nedeni inceleme sürelerinin
getirilen son teknikler ile (yeni sekans tipleri ve software
modifikasyonları ile) 15-20 dakikadan 1 dakikanın altına
indirilmesidir. MRGde tekniklerin bu derece geliştirilmiş
olmasıyla birlikte toraks ve abdominal MR incelemeleri hala
optimal değildir. MRGde kontrast maddeler konusu şu
ana kadar çok büyük aşamalar kaydedememiş olsa da, dünyada
birçok merkezde özellikle kontrast maddeler konusu üzerinde çalışılmaktadır.
Kontrast maddelerin aktif biçimde kullanılmaya başlanması
ile MRGnin bugün için optimal olmayan incelemelerinin, çok
başarılı inceleme yöntemleri haline gelmesi
beklenmelidir. MRGde kontrast maddelerin uygulanmaya başlanması
ile dokular arasnıda dinamik fizyolojik bilgi ile birlikte, yüksek
anatomik detay da elde edilebilmektedir. Bu sayede sintigrafinin
anatomik detay yetersizliğini ve BTnin fizyolojik bilgi
yetersizliğini ortadan kaldırmaktadır. Aslında
MRGnin ilk yıllarında yaygın olan görüş,
MRGnin kontrast maddeye ihtiyacı olmadığı
şeklindeydi. Ancak özellikle son yıllarda optimal
inceleme için MRG incelemelerinde kontrast maddenin gerekliliği
hususunda ortak görüş mevcuttur.
MRG görüntülerinde, daha önce detaylı olarak tartışıldığı
gibi, sinyal intensitesini belirleyen unsurlar dokuların
relaksasyon zamanları (T1, T2) ve proton dansitesidir;
MRGde kontrast maddeler protonların relaksasyon zamanlarını
kısaltarak veya proton dansitesini değiştirerek
etkili olurlar (Şekil 9.1).
 |
|
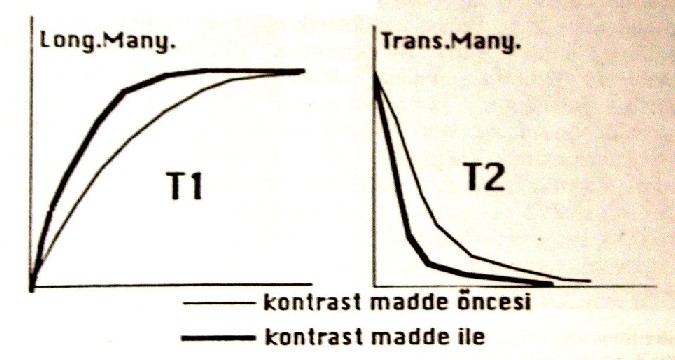
Sekil 9.1:
Kontrast maddelerin etkinligi T1 ve T2 relaksasyon
surelerinin kisalmasi ile iliskilidir. Kontrast
maddelerin kullanilmasi ile T1 ve T2 relaksasyon
egrilerinin kisalma yonunde yer degistirdigine dikkat
ediniz. |
|
| Bu
başlık altında bahsedilecek çoğu madde bugün
için klinik kullanıma sunulmamıştır. Bununla
birlikte çoğu MRG araştırma merkezlerinde, özellikle
bu kontrast maddelerin etkinliği ve yeni geliştirilebilecek
kontrast maddeler üzerinde çalışılmakta olup, önümüzdeki
çok kısa zaman içersinde, MRG klinik kullanımına
sunulacak çeşitli kontrast maddeler ile çok daha etkin rol
oynayacaktır.
Kontrast madde protonlar arasına yayılınca nükleer
relaksasyonları stimüle eder ve T1 ve T2 relaksasyon
zamanlarını kısaltır. T2 ve T2* daki kısalma
mikroskobik manyetik çevrede inhomojenitenin artması ile
kolayca açıklanabilir. T1deki kısalma ise,
dipole-dipole interaction ile açıklanmaktadır
[45]. Temelde MRGde kullanılan kontrast maddeler kimyasal
olarak 2 grupta toplanabilir:
a
- Paramanyetik elementler
b
- Ferromanyetik elementler (superparamanyetik)
Paramanyetik iyonlarda nükleusların çevrelerinde bulunan
elektronlar (karşılıklı dönen elektronlar
olarak) eş değildir, ve bugün için bunlardan en çok
bilineni gado-pentetate
dimeglumine dir (7 tane çiftleşmemiş elektron
içerir) [45]. Ferromanyetik materyallerden bugün için en çok
bilineni ise paramanyetik
iron (demir) dir (süperparamanyetik materyaller bu grup
içinde incelenmektedir).
|
|
 |
|
Resim:
Sıklıkla
kullanılan MR kontrast
maddelerinden "Magnevist" |
|
 |
|
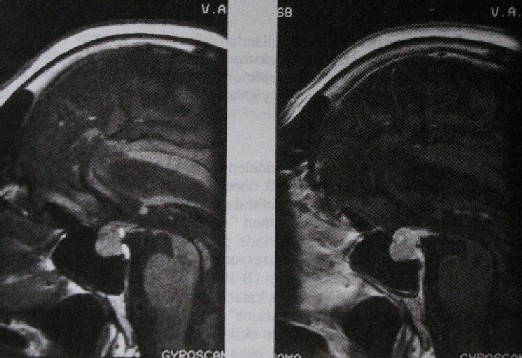
Resim
9.1: T1 agirlikli (TR:600, TE:18) kontrast oncesi ve
sonrasi sagittal goruntulerde hipofiz kaynakli tm kitlesi
kontrast verilmesini takiben belirgin boyanma gostermektedir.
Kontrastli kesitlerde tumor kitlesinin cevre yapilara
uzanimi daha net izlenmektedir (Gd-DTPA) |
Kontrast maddelerin T1 ve T2
sürelerini kısaltmaları intensiteyi nasıl etkiler?
T1deki
kısalma intensitenin artmasına, T2deki kısalma
ise intensitesinin azalmasına neden olmaktadır (Şekil
9.1 de T1 ve T2 eğrilerinin kontrast madde ile ne yönde yer
değiştirdiklerine dikkat ediniz). Bununla birlikte,
kontrast maddelerin (bazı faktörlere bağlı olmak
üzere) T1 veya T2 üzerine olan etkileri eşit değildir;
T1 veya T2 üzerine olan etki diğerine göre daha fazla
olmaktadır. Hangisinin daha dominant olacağını
bir çok faktör belirlemektedir (TR ve TE parametreleri, magnetin
gücü [Tesla], kontrast maddenin cinsi ve miktarı gibi).
Örneğin; süperparamanyetik iron oxide özellikle T2
süresini etkilemektedir; dolayısıyla bu kontrast
maddenin etkisi en iyi şekilde T2 ağırlıklı
görüntülerde izlenir.
Bunun tersi olarak uygun dozlardaki
paramanyetik gadopentetate dimeglumine özellikle T1
süresini etkilemekte ve kontrast maddenin etkisi en iyi şekilde
T1 ağırlıklı görüntülerde izlenmektedir;
ancak aynı kontrast madde yüksek dozlarda uygulandığında
T2 üzerine olan etki T1 üzerine olan etkiden daha belirgin
olmakta, bunun sonucu olarak da kontrast maddenin etkisi T2 ağırlıklı
görüntülerde daha iyi izlenmektedir. Magnet gücü (Tesla)
pratikte bunlar kadar etkili olmasa da bazı durumlarda
kontrast etkisini değiştirebilmektedir; örneğin
gadopentetate dimegluminenin etkisi 0,02 Tesladan 1,5
Teslaya çıkıldığında yaklaşık
1/3 oranında azalmakta ve 0,15 Tesladan düşük değerli
magnetlerde Gd-DOTA (gadolinium tetra-azacyclododecane
tetra-aceticacid) T1 üzerine gadopentetate dimeglumineden
daha etkili olmaktadır.
MRGde
kontrast maddeleri sınıflandırırsak;
a-
Ekstrasellüler ajanlar
b-
Hepatobiliyer kontrast ajanlar
c-
Vasküler ajanlar
d-
Retiküloendotelial ajanlar
e-
Lenfografik ajanlar
f-
Oral gastrointestinal ajanlar
g-
Tümör spesifik ajanlar.
Ekstrasellüler
ajanlar
Bu grupta gadopentetate
dimeglumine günümüzde prototip olarak bilinir; bununla
birlikte Gd-DOTA meglumine (Guerbet Lab.) [47] ve Ferrioxamine (Salatur) [46] de bu gruba girmektedir ve bunlar
üzerinde klinik deneyler halen devam etmektedir. Bunların
doku spesifisitileri yoktur ve biyolojik toksisitelerini azaltmak
için chelat halinde hazırlanırlar. Bu maddelerin
fizyolojik ekstrasellüler dağılımları
birbirinden çok az farklılıklar gösterir (Ferrioxaminein
hepatik ekskresyonu diğerlerine göre biraz fazladır). Gadopentetate
dimeglumine I.V. olarak uygulandığında
plazma yarı ömrü 90 dakikadır ve % 90ı 3 saat
saat içinde böbrekler tarafından atılır. ABDda
tavsiye edilen doz 0,1 mmol/kg. olmakla birlikte, 0,2 mmol/kg.
olarak da kullanılabilmektedir. Bugüne kadar çok az sayıda
ciddi reaksiyonlar haricinde klinik olarak oldukça güvenli
olarak kabul edilmiştir. Hayvanlar üzerinde yapılan çalışmalarda
hızlı infüzyonun ilacın yan etkilerini artırmadığı
bulunsa da, genellikle yavaş infüzyon tavsiye edilmektedir.
Gadopentetate dimeglumine in hiperosmolar olmasına bağlı
görülebilen yan etkileri azaltmak için isoosmolar non-ionik
formülasyonlar olmasına bağlı görülebilen yan
etkileri azaltmak için isoosmolar non-ionik formülasyonlar geliştirilmiştir:
Gd-DTPA-bis-methylamide,
Gd-HP-DO3A.
Bu kontrast maddeler (Radyolojide kullanılan diğer
iyonik kontrast maddeler gibi) hızlı biçimde vasküler
kompartımandan ekstrasellüler sahaya geçip, pasif glomerüler
filtrasyon ile böbrekler tarafından itrah edilirler. Dolayısıyla
Gradiyent-eko gibi hızlı sekanslar kullanılarak
dinamik çalışmalar yapılabilmektedir.
 |
|
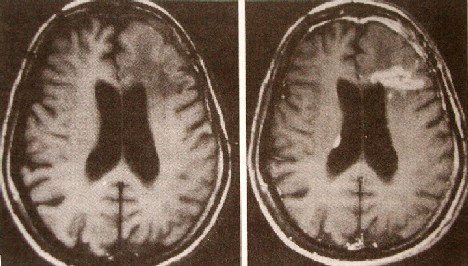
Resim
9.2: SE sekansi (TR:600, TE:20) ile elde edilmis
goruntulerde kontrast oncesi goruntude sinirlari net olmayan
hipointens saha icinde, kontrastliu goruntude beligin
hiperintens yer kaplayici lezyon izlenmektedir (rekurrens
glial tumor). Ayrica sag ventrikul kenarinda metastatik
nodul dikkati cekmektedir. |
Hepatobiliyer
kontrast ajanlar
Bu grup içinde incelenen kontrast maddelerin temelinde, bu
maddelerin hepatositlere afinitesi söz konusudur. Bu amaçla ilk
önce Fe-EHPG denendi; bununla birlikte hayvanlar üzerinde yeterli
hepatosit afinitesi göstermemesi ile klinik kullanıma ulaşamadı
[49]. Mn-DPDP ve
gadoloniumun octadentate chelate formu (B-19036)
gibi yeni geliştirilen formülasyonlar üzerinde çalışmalar
hızla sürmektedir. B-19036 ile yapılan deneylerde safra
yollarına ekskresyon gadopentetate dimeglumine ile karşılaştırıldığında
daha yüksek bulunmaktadır (B-19036 ile 14,6, gadopentetate
dimeglumine ile 7,6 mmol) [48]. Bunların yanında karaciğer
patolojileri için günümüzde klinik kullanımda olan
gadopentetate dimeglumine gibi ekstrasellüler kontrast
maddeler kullanılabilir; ancak bunların karaciğerden
ekskresyonu, geliştirilmeye çalışılan
hepatobiliyer formülasyonlara göre çok düşük, buna bağlı
olarak da karaciğer patolojilerinde başarı düşüktür.
Vasküler
ajanlar
Bu grup içindeki kontrast maddelerin özelliği vasküler yapılarda
(kanda) hızlı biçimde yayılması; ancak
ekstrasellüler aralığa geçmemesidir. Bu amaçla en çok
bilinen madde, serum albuminine kovalen bağlarla bağlanmış
gadopentetate dimegluminedir [50]. Bununla birlikte şu
ana kadar yapılan tüm çalışmalar hayvan deneyleri
üzerinde olup, henüz klinik değerleri tam olarak
bilinmemektedir.
Retiküloendotelial
ajanlar
Bu grupta I.V.olarak uygulandıktan sonra RES tarafından
elimine edilen maddeler incelenmektedir. Bu amaçla en çok
bilinenler, paramanyetik iyonlar içeren liposome
ve superparamanyetik iron oxide in dextran kristalleridir.
Iron oxide karaciğer, dalak ve kemik iliği gibi
RES dokularında doz ile direk ilişkili olarak sinyal
intensitesinde azalmaya neden olmaktadır ve bu en iyi şekilde
T2 ağırlıklı görüntülerde izlenebilmektedir.
Bugüne kadar yapılan deneyler Iron oxide in yavaş
infüzyonlarında yan etki oluşturmadığını,
hızlı infüzyonlarında ise ciddi hipotansiyonlara
neden olabildiğini göstermektedir. Özellikle bu grupta
incelenen maddeler klinik kullanıma sunulduğunda
MRGnin etkinliğinin çok fazla artması beklenmelidir.
Lenfografik
ajanlar
Bu
amaçla subkutan olarak yine superparamanyetik iron oxide
denenmekte olup, kontrast madde bölgeyi drene eden lenf nodlarında
birikmektedir.
Oral
gastrointestinal ajanlar
Şu ana kadar bahsedilen tüm
kontrast maddeler oral olarak kullanıldığında
gastrointestinal sistemin belirlenmesinde etkili olduğu
bilinmektedir. Bunun haricinde mobil proton preparatları (gaz
veya barium şeklinde) ve kısa T1 preparatları (paramanyetik
ferric ammonium citrate) üzerinde çalışılmaktadır.
Tümör
spesifik ajanlar
Paramanyetik kontrast ajanlar tümör fokusunu belirlemede
superparamanyetik kontrast ajanların etkili olması
beklenmektedir ve bu konuda da çalışmalar sürmektedir
[72].
Ana
sayfa I Bir
Önceki Bölüm
I
Bir Sonraki Bölüm
I iletisim I
www.birthmarks.us
|
